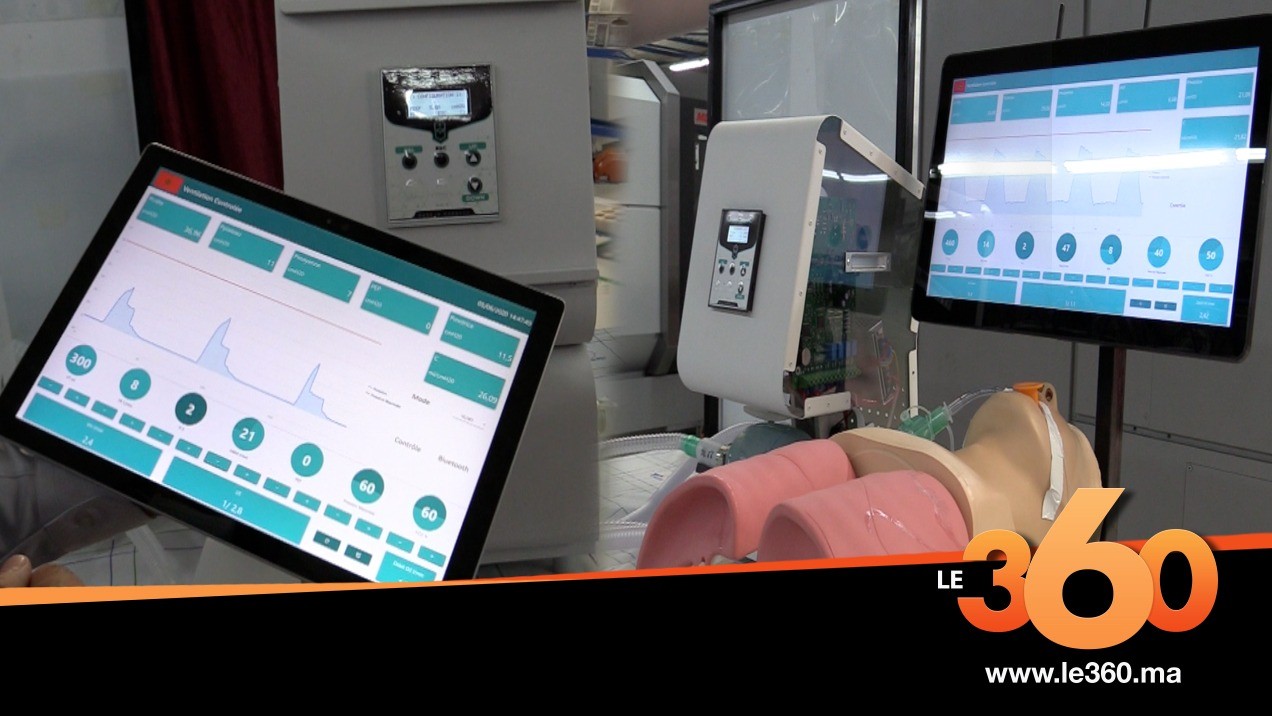
Dans un précédent article, publié samedi 22 août dernier, sur la base de témoignages recueillis auprès des différentes parties prenantes, Le360 avait pointé du doigt les nombreuses complications administratives à l’origine du retard de livraison d’un premier lot de 400 respirateurs, commandés par le ministère de la Santé, fabriqués par le consortium SERMP-Aviarail. Ces deux opérateurs constituent le noyau dur du collectif fédéré autour de ce projet, composé d’une quinzaine d’entreprises opérant dans les secteurs de l’ingénierie, de l’aéronautique, de l’automobile et de l’électronique.
La chronologie des faits, révélés par notre article, ont montré l'immense labyrinthe bureaucratique des services du ministère de la Santé auquel les promoteurs du projet ont été confrontés. Alors même que le Maroc connaît depuis quelques semaines une sévère remontée des cas de Covid-19, les professionnels de la santé n’excluant pas une saturation des unités de réanimation et de soins intensifs, accompagnée d’une pénurie d’équipements médicaux, dont des respirateurs.
Dans une note parvenue à la rédaction ce mardi 25 août, le ministère de la Santé se dit mobilisé pour encourager la fabrication locale de respirateurs artificiels.
«A la lumière de l’évolution de la situation sanitaire au Maroc et croyant à l’importance de ce sujet, le ministère de la Santé accompagne la société qui fabrique le respirateur artificiel afin de pouvoir le mettre en service tout en s’assurant qu’il sera sûr, performant et de qualité, et procéder à son enregistrement comme dispositif médical», précise cette note.
A cet effet, poursuit le document, la Direction du médicament et de la pharmacie (DMP) a recommandé, après vérification des documents fournis par le fabricant de:
1- déclarer la société en tant qu’établissement de fabrication de dispositifs médicaux;
2- produire une déclaration de conformité du produit selon les normes exigées;
3- préciser le fabricant légal du dispositif médical et les sous-traitants (contrat de sous-traitance);
4- documenter le procédé de fabrication et les contrôles entretenus en amont et en aval (Tests de validation et contrôles de libération);
5- fournir une documentation technique incluant essentiellement:
• une investigation clinique sur le respirateur démontrant la sécurité et l’efficacité du dispositif;
• les spécifications de la matière première et ses origines;
• les rapport de validation des procédures et les équipements des locaux
• les procédés de stérilisation et le rapport de validation;
6- s’engager pour une certification ISO 13485 ou une norme garantissant le respect des bonnes pratiques de fabrication;
7- préparer un projet d’étiquetage du dispositif médical.
Cette même note indique que les services du ministère de la Santé, chargés de l’enregistrement des dispositifs médicaux, n’ont reçu à ce jour aucune demande officielle d’obtention de certificat d’enregistrement de ce dispositif.
«Seuls des documents présentant le produit et des essais précliniques sur l’animal (une seule Brebis) ont été transmis par email», souligne-t-on du côté du département ministériel dirigé par Khalid Aït Taleb.
Réagissant à cette dernière remarque, les promoteurs du projet expliquent que le ministère de la Santé leur a imposé, lundi 17 août dernier, une nouvelle procédure digitalisée, laquelle nécessite l’enregistrement préalable du fabricant SERMP en tant qu’entreprise médicale.
Au-delà de ce véritable marathon procédural, du reste totalement justifié d’un point légal, ce qui est le plus reproché au ministère de la Santé, c’est surtout son manque de proactivité, voire d’agilité, pour accélérer les démarches qu'il demande, à un moment où l’inquiétude d’une deuxième vague pandémique se fait de plus en plus ressentir.
A simple titre d’exemple, à quoi sert-il d’insister sur la modification immédiate des statuts de l’entreprise (pour intégrer l’activité des dispositifs médicaux) alors même que les tribunaux sont en vacances judiciaires?
Il convient de rappeler que l’initiative du collectif créé autour de ce projet ne revêt nullement un caractère lucratif. Les dirigeants de SERMP et Aviarail ont à maintes reprises affirmé que les respirateurs seront proposés à prix coûtant. Puis, lors du lancement de la phase industrielle début avril dernier, suite à la réception du bon de commande du ministère de la Santé (400 unités), à aucun moment on ne leur a demandé de procéder à des essais cliniques ou de justifier un certificat d’enregistrement en tant qu’entreprise médicale.
«Ces industriels se sont lancés dans la fabrication d'un respirateur à 100% marocain pour répondre aux besoins les plus urgents de la population, conformément aux instructions du Roi Mohammed VI. Ils ne pouvaient en aucun cas anticiper cette armada de procédures», soutient un membre de ce collectif.
Moralité: les promoteurs du projet n'ont pas besoin d'une réponse administrative de la part du ministère de la Santé, mais plutôt d’un accompagnement, main dans la main.
Il ne s’agit pas de contourner les procédures, mais surtout de faire preuve d’agilité dans les circonstances exceptionnelles que le pays traverse. Un simple engagement sur l'honneur de compléter les démarches requises, parallèlement à la livraison des respirateurs, aurait d'ailleurs amplement suffi, pour résoudre le problème.